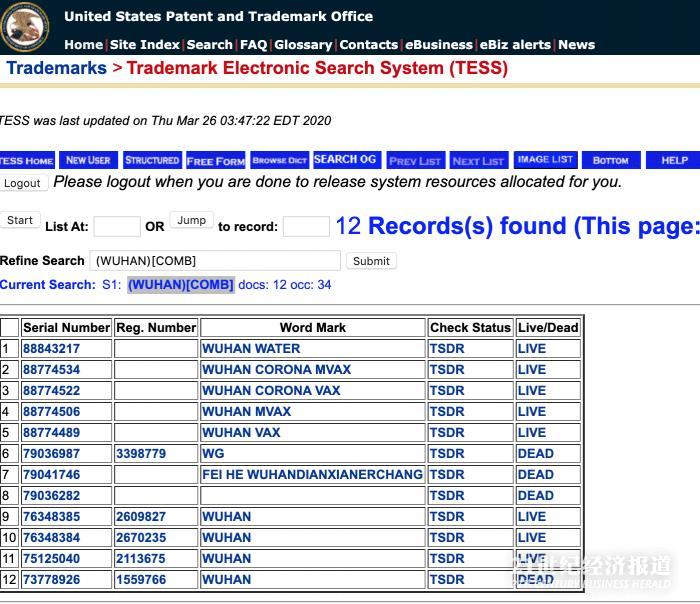
商标申请时间为2020年1月27日。...
成立于2010年、总部位于位于美国马萨诸塞州剑桥的生物技术公司Moderna是此次新冠肺炎(COVID-19)疫情中的“明星”企业。
2020年3月16日,美国国立卫生研究院(NIH)宣布已对Moderna研发的疫苗mRNA-1273的第1期研究的首位参与者给药,从序列选择到首次人类给药共63天。
根据美国专利商标局网站显示,Moderna将其新冠疫苗产品商标申请为WUHAN CORONA VAX和WUHAN CORONA MVAX(武汉新冠)。
二者的申请时间均为2020年1月27日。
1月27日WHO还未公布新冠肺炎疫情的新命名。
2020年2月11日,国际病毒分类委员会宣布造成此次疫情的病毒(此前称为“2019新型冠状病毒”)及其引发的疾病的正式名称为:
疾病:2019冠状病毒病(COVID-19)
病毒:严重急性呼吸综合征冠状病毒2(SARS-CoV-2)
新病毒命名为“严重急性呼吸综合征冠状病毒2(SARS-CoV-2)”。选择这一名称是因为这一病毒与导致2003年SARS疫情的冠状病毒在基因上相互关联。这两个病毒虽然相关,但却是不同的病毒。
为什么病毒和疾病有不同名称?
病毒及其引起的疾病通常都有不同名称。例如,人类免疫缺陷病毒(艾滋病毒)是导致艾滋病的病毒。人们通常知道麻疹(measles)等疾病名称,但不知道引起这一疾病的病毒(rubeola)的名称。
病毒和疾病有不同的命名程序和用途。
病毒按遗传结构命名,这样做的好处是便于诊断试剂、疫苗和药物开发。病毒学家以及广泛科学界人士负责此项工作,所以,病毒由国际病毒分类委员会(ICTV)命名。
而疾病命名是为了便于讨论疾病的预防、传播、传播力、严重性和治疗。世卫组织负责人类疾病的预防和应对工作,因此,疾病由世卫组织在《国际疾病分类》(ICD)中正式命名。
Moderna做了什么?
根据Moderna公布的时间线,2020年1月11日,中国对外分享了新型冠状病毒的基因序列。
2020年1月13日,美国国立卫生研究院(NIH)和Moderna的传染病研究小组确定了该公司针对新型冠状病毒的疫苗mRNA-1273的序列。当时,美国国立卫生研究院(NIH )的国家过敏和传染病研究所(NIAID)披露了他们打算使用mRNA-1273疫苗应对冠状病毒威胁进行一项1期研究的意图,而Moderna已动员用于临床生产。该批次的生产由流行病预防创新联盟(CEPI)资助。
然后在1月27日进行了上述商标申请。
2020年2月7日,完成了第一批临床试验,包括小瓶的填充和完成,从序列选择到疫苗生产共计25天。然后将该批次进行分析测试以释放。
2020年2月24日,该临床批次从Moderna运送到NIH,用于其1期临床研究。
2020年3月4日,美国食品药品监督管理局(FDA)完成了对NIH针对mRNA-1273的研究用新药(IND)申请的审查,并允许该研究继续进行临床试验。
2020年3月16日,NIH宣布已对mRNA-1273的第1期研究的首位参与者给药,从序列选择到首次人类给药共63天。这项1期研究将提供有关mRNA-1273的安全性和免疫原性的重要数据。免疫原性是指疫苗诱导参与者免疫反应的能力。这项开放性试验预计将在大约六周内招募45名18至55岁的健康成人志愿者。
2020年3月23日,Moderna提交了最新报告,其中包括有关获得针对COVID-19的疫苗的潜在时机的信息。该公司报告说,第一阶段研究正在按照协议在NIAID的指导下进行。该公司进一步报告说,虽然市售疫苗不可能在至少12-18个月内上市,但在紧急使用情况下,有可能在2020年秋季向某些人(包括医疗保健专业人员)提供疫苗。任何紧急使用均应获得合适的监管机构的批准,基于出现的mRNA-1273临床数据将支持在许可之前使用疫苗。此外,该公司证实,它正在扩大生产能力。如之前所披露的,每月生产数百万剂的能力取决于扩大规模投资以及公司现有制造基础设施的进一步扩建。
根据Moderna自己的介绍,其业务专注于开发可用于多种疾病和病症的mRNA药物。包括治疗传染病、癌症、罕见疾病和心血管疾病的新型mRNA药物,但目前没有药物获批上市。
Moderna对一些常见问题进行了回应。
mRNA平台的验证程度如何?
mRNA是新兴的平台。在过去的几年中,我们已经在临床试验中证明了其在超过1,000名受试者中的疫苗潜力。这包括针对其他五种呼吸道病毒(两种大流行性流感病毒株,RSV,hMPV和PIV3)成功的早期(阶段1)临床试验。在过去的四年中,我们已经针对mRNA疫苗启动了9项临床试验。但是,必须强调的是,我们还处于早期。我们最先进的疫苗计划(CMV)处于2期临床测试中,迄今为止我们还没有批准的药物。
曾经研究过其他冠状病毒吗?
我们之前曾与NIH合作开发了针对MERS-CoV的疫苗,该疫苗是与当前大流行不同的一种冠状病毒。尽管该程序还处于研究阶段,但在我们为mRNA-1273开展研究时,它提供了重要的见识。在对mRNA-1273进行1期研究之前,我们之前尚未在人类中测试过冠状病毒疫苗。
mRNA-1273如何能够如此迅速地运动?
mRNA是一个信息分子,我们使用病毒的序列而不是通过对病毒本身的作用来设计我们的mRNA疫苗。我们的mRNA平台在基础科学,制造和临床开发方面在速度和效率上均具有显着优势。
Moderna目前在其预防性疫苗形式中有9个开发候选对象。迄今为止,Moderna已展示出针对6种预防性疫苗(H10N8,H7N9,RSV,基孔肯雅病毒,hMPV / PIV3和CMV)的阳性1期数据读数。
对于mRNA-1273,我们能够利用我们在疫苗方面的经验迅速进行1期临床试验材料的设计和制造。这包括我们迄今为止对1,000多个主题对平台安全性的广泛理解。我们还受益于我们完善的制造能力,在过去的两年中,该能力生产了100批用于人类临床试验的mRNA药物。
有关针对此次新冠肺炎疫情的疫苗mRNA-1273的问题:
第一阶段后会发生什么?
NIH正在运行的试验的1期安全性和免疫原性数据有望指导我们的下一步。鉴于这种大流行,我们已经开始并行开展工作,以负责任的方式促进进一步发展。
公司正在根据自己的研究性新药(IND)文件积极准备潜在的2期研究,以美国国立卫生研究院正在进行的1期研究数据为基础。为了在持续的全球公共卫生紧急情况下继续开发这种潜在的疫苗,Moderna打算与FDA及其他政府和非政府组织合作,为第二阶段和随后的任何试验做好准备,预计将进行更多的试验。受试者,并将寻求产生其他安全性和免疫原性数据。正在为潜在的2期试验生产mRNA-1273材料,该过程可能在几个月内开始。我们的目标是生成能够证明mRNA-1273抵抗SARS-CoV-2感染的安全性和有效性的数据。
是否正在进一步提供疫苗?
Moderna已经开始为快速提高其制造能力做准备,如果mRNA-1273被证明是安全的并具有预期的收益,那么它可能允许未来制造数百万剂。我们会全天候工作,以确保尽快广泛地提供疫苗。