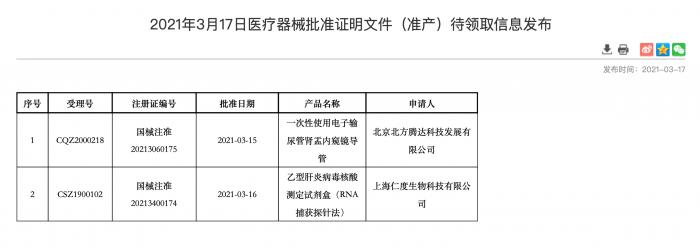
21世纪经济报道记者获悉,近日,上海仁度生物科技股份有限公司(下称“仁度生物”)自主研发的全自动高敏HBV RNA定量产品获得国家药品监督管理局(NMPA)发布批件正式上市(注册证号:国械注准20213400174),成为国内乃至全球首个应用上市的HBV RNA定量产品。
仁度生物自主研发的HBV RNA是第一个进入优先审批通道(2019年4月),也是第一个获得国家药监局批准上市,正式用于临床的(2021年3月17日注册证号公布)产品。该产品的获批,标志着第一个由中国率先应用到临床的乙肝新指标诞生(现有乙肝指标均是由国外首先应用到临床)。
目前我国大约有2000-3000万的慢性乙肝病人,常规来讲每个病人一年要测4次,每年大约有8000-12000万的检测需求量,以此推算,市场需求巨大。
记者了解到,新指标HBV RNA与现有的HBV DNA和HBsAg指标对比,临床医疗应用意义重大,大量循证医学证据表明乙肝新指标HBV RNA具有广泛的临床应用前景,有力的弥补了传统乙肝临床诊疗指标(如HBV DNA和HBsAg)的不足,尤其在:(1)疗效监测,精准反映治疗疗效和病情进展;(2)早期预测干扰素治疗效果,指导治疗方案选择和调整;(3)评估停药复发风险,指导后续治疗方案等方面具有重要的指导价值。
公开资料显示,仁度生物成立于2007年,位于上海张江医疗器械园,是国内首家专注于RNA分子诊断技术与产品的上海市高新技术企业,致力于开发、推广以实时荧光恒温扩增检测技术(简称SAT技术)为基础的RNA分子诊断产品。公司拥有从诊断试剂到全自动配套仪器研发和制造的一整套核心技术,产品覆盖优生优育、手足口病、呼吸系统病原体、食品安全、血液检测等领域。
目前,仁度生物已有注册产品19个,其中三类注册产品13个,其中4项被认定为上海市高新技术成果转化项目,3个产品进入国家及上海市的创新产品推荐目录,1个产品被评为上海市生物医药创新产品。国内首创的全自动核酸检测分析系统也已获批上市,公司产品在500多家医疗机构使用,70%为三甲医院。
值得一提的是,目前,仁度生物正在冲刺科创板上市,此前2020年11月4日,仁度生物与中金公司签署上市辅导协议,并于同日在上海证监局备案。
(作者:朱艺艺 编辑:朱益民)