预计辉瑞将在2月初公布授权合作的企业。
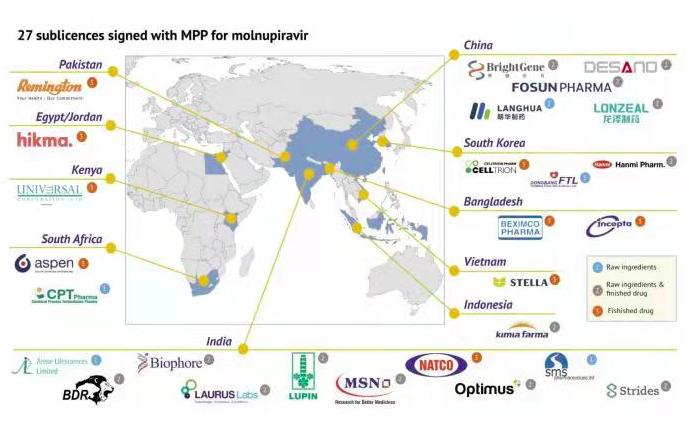
21世纪经济报道记者 季媛媛 上海报道 1月20日,日内瓦药品专利池组织(Medicines Patent Pool, MPP)宣布,已与包括复星医药(600196)、博瑞医药(688166)、迪赛诺医药、朗华制药、龙泽制药在内的全球27家企业签订协议,将为全球105个中低收入国家或地区生产及供应高质量、可负担的默沙东口服抗新冠病毒药物Molnupiravir仿制药。
受此消息影响,今日(1月21日)A股开盘,复星医药、博瑞医药皆涨停。
1月21日中午,博瑞医药发布公告称,根据协议,除了专利许可使用费,产品授权各方不享受产品销售分成,根据购买方性质的不同,公司应按照该产品年度净销售额(定义依据协议)的5%或10%向默沙东支付专利许可使用费,但基于MSD-MPP协议,前述专利许可使用费将自WHO宣布COVID-19不再被列为“国际关注的突发公共卫生事件”的次月起开始收取。
此外,本次许可项下合作药品的生产前,尚需完成相关技术交接;生产设施需经SRA(严格监管机构,包括国际人类用药技术要求协调理事会(ICH)成员、或ICH观察员及与ICH成员相关监管机构等)批准或经世界卫生组织预审合格。本次许可项下合作药品在区域内的生产、销售等,须待相关主管机构批准(包括但不限于上市批准)后方可实施。公司于本次许可下生产的合作药品在区域内能否获得当地药品监管机构上市批准、于区域内的上市时间存在不确定性。
当前新冠病毒仍在全球大流行,新变种奥密克戎已经在全球150多个国家和地区传播,并且在多国已成为主要流行株。其中,中国已经有14个省份报告奥密克戎输入病例,而天津、河南、深圳等地还出现了本土奥密克戎疫情。
新冠口服特效药被认为是有望成为终结疫情的最后一张“拼图”,此次虽然有5家中国企业获得仿制许可,但是作为全球最大的发展中国家,这些企业生产的默沙东新冠口服药仿制药将不会在中国市场上市销售,为什么中国不在受惠国名单之列?
此次仿制药为何不能在中国市场销售?
21世纪经济报道记者通过查询相关论文资料获知,药品专利池(MedicinesPatent Pool, MPP)是2010年在瑞士日内瓦成立的。MPP通过与原研药企就药品专利的自愿许可进行谈判,原研药企将其药品专利放入专利池中,仿制药企向MPP申请获得专利池中的专利实施许可,生产并向中低收入国家供应仿制药。
仿制药企(主要面向发展中国家制药企业)一是自愿将其相关药品专利纳入MPP;二是自愿向MPP提交被许可意向,被许可意向经MPP专家评议通过后,MPP与仿制药公司签署许可协议,向原研公司给付许可费并向MPP支付中介费。获得再许可的仿制药企可被允许在发展中国家生产原研公司的专利药品, 并依照许可协议规定,将所生产的专利药品销往低等和中低等收入国家。MPP许可为非独占许可,并常通过许可多家仿制药企业来增加市场竞争,降低药品价格。概而言之,MPP平衡了原研公司与仿制药商之间的利益,且有效解决了患者的药物可及性问题及其与生命健康权之间的冲突问题。
此外,MPP许可有市场限制。再许可主要面向131个低等和中低等收入国家,但不包括中国、欧美等重要市场,意在将原研公司“放弃”的市场分享给仿制药企。且不同药品销往的国家和地区有所不同。像巴西和中国这样的大市场通常不被列入许可销售的地理范围内。比如,从MPP网站公开的信息显示,此前有三家中国药企获得了关于富马酸替诺福韦二吡呋酯(TDF)的MPP许可,根据许可协议,中国药企生产的TDF仿制药(包括含有TDF组合制剂)可以销往112个国家,但中国不在其列。2017年9月,吉利德与MPP修改了关于替诺福韦艾拉酚胺(TAF)的许可协议。与原来的协议相比,许可销售国家范围扩大至116个国家。但有36个中等收入国家被排除在许可协议的地理范围外。
现有的MPP许可覆盖共达131个国家,涵盖世界银行标准下所有低收入国家和50%-80%的中等收入国家。
按世界银行2021年7月发布的最新标准,高收入国家为人均GNI(国民总收入)超过12695美元;中等偏上收入国家人均GNI超过4096美元,但低于12695美元;中等偏低收入国家人均GNI在1046美元到4096美元之间;人均GNI低于1046美元的,均属于低收入国家。根据2021年中国经济年报,2021年我国人均GDP达到80976元,按年平均汇率折算,已突破1.2万美元,而GDP与GNI差距很小,如此对照中国应在中等偏上国家之列。
中国患者何时能用上新冠口服药?
默沙东方面表示,截至2021年底已生产了1000万疗程,预计2022年将至少生产2000万疗程。截至目前,默沙东已经向获得上市批准或使用授权的20多个国家/地区运送Molnupiravir,已经有患者开始接受该药物进行治疗。为了增加已获许可的仿制药制造商的供应量,默沙东已经与联合国儿童基金会达成一项协议,在2022年上半年向中低收入国家/地区调配总计300万疗程Molnupiravir。
但事实上,新冠口服治疗药物供应量远不能满足需求量。据悉,辉瑞的Paxlovid需要6到8个月的生产时间。辉瑞与美国政府签订协议中的首批1000万剂疗程需到6月才能交付。默沙东表示,1月底将能交付300万剂疗程的Molnupiravir;,但因默沙东的药物疗效较低,需求有所减少。
据中泰证券报告,美国卫生与公众服务部数据显示,自2021年9月以来,全美截至目前共分发抗新冠病毒药物近300万,包括257万剂抗体注射药物及36万疗程口服药物。其中,默沙东口服药则占总分发口服药数量83%,合计分发30万疗程,但近期全美新增确诊日均150万例左右,远远供不应求。
此外,有消息人士对21世纪经济报道记者透露,预计辉瑞将在2月初公布授权合作的企业,为全球中低收入国家或地区生产及供应高质量、可负担的口服抗新冠病毒药物Paxlovid仿制药。
此前辉瑞已与联合国支持的非营利组织MMP达成了自愿许可协议。获得MPP授权的合格仿制药生产商将能够向95个中低收入国家以更低的价格提供该药。
国盛证券也分析,当前企业申请辉瑞的MPP许可应该也都已经递交了。根据科伦药业平台上回复投资者的问答,科伦递交了申请,其他企业递交的情况暂时无法确定。在此之前,雅本化学因“向辉瑞供应卡龙酸酐”的传闻而持续大涨,但后被公司否认,目前公司仍在停牌当中。金城药业也因中间体一度大涨。
至于此次错过了默沙东Molnupiravir仿制药许可机会的企业,还有谁能拿下辉瑞的Paxlovid仿制药授权。
虽然MPP许可生产的默沙东及后续的辉瑞新冠口服药仿制药无法在中国市场销售,但是对中国患者影响不大。对此有证券分析人士对21世纪经济报道记者指出,一是中国疫情控制得比较好,患者数量少需求本身就少;二是国产新冠口服药进展也很快,预计今年可提交上市申请。
此前,国产新冠口服药VV116已在乌兹别克斯坦获紧急使用授权。有市场消息认为,在通过临床试验后,君实生物有望在2022年下半年申请VV116上市。对此,君实生物在接受21世纪经济报道记者采访时表示,公司目前正在积极推进VV116的临床试验,正在准备该药物国际多中心二、三期临床试验。
除了君实生物,国产在研新冠口服药还包括开拓药业AR拮抗剂普克鲁胺目前处于全球三期临床中,此前已在巴拉圭获批EUA;真实生物阿兹夫定目前正在中国、巴西、俄罗斯开展III期临床试验,初步数据良好;前沿生物美国I期临床正在进行;先声药业针对SARS-CoV-2 病毒复制必须的关键蛋白酶3CL,在临床前动物模型上显示了良好的抗病毒活性和安全性;云顶新耀宣布与新加坡公共研发机构达成合作协议,引进其新冠口服药EDDC-2214。
MPP供应协议将对哪些企业产生利好?
这个供应协议,除了复星医药,也让博瑞医药成为了一大赢家。
博瑞医药2021三季报显示,公司主营收入7.48亿元,同比上升46.62%;净利润1.77亿元,同比上升45.3%。而在1月初,博瑞医药披露公告,公司拟以1000万元认购江苏保易制药有限公司人民币116.67万元的新增注册资本。增资完成后,公司直接持有保易制药3.92%股权,保易制药不纳入公司合并报表范围。博瑞医药拟与保易制药在订单生产及产品研发方面展开合作,以整体提升公司制药技术综合能力,完善“起始物料→高难度中间体-→特色原料药→制剂”的全产业链布局。
此外,博瑞医药披露,公司在产能方面,截至2021年三季度末,泰兴基地进度为81.5%、苏州项目已完成桩基和支护工程,印尼项目土建完成率95%。
据民生证券指出,辉瑞Paxlovid国内合作供应商为博腾股份、凯莱英等;默沙东Molnupiravir国内合作供应商为天宇股份、博腾股份等,美国政府已经订购了1000万疗程辉瑞药物和300万疗程默沙东药物,预计全球订单量将进一步增长。
某医药行业首席分析师对21世纪经济报道记者表示,也是受到此次MMP协议的推动,原料药、CDMO供应商也会迎来了多番利好。在五家本土药企获默沙东口服药仿制许可,为全球105个中低收入国家或地区生产及供应新冠口服药Molnupiravir仿制药后,这意味着,后续原料药、CDMO供应商将继续放量。
此前,中国医药保健品进出口商会分会秘书长朱仁宗在接受21世纪经济报道记者采访时表示,从2020年吉利德“瑞德西韦”开始,中国原料药、CXO企业或多或少已经加入到新冠肺炎治疗药物研发链条中,承接新冠肺炎相关治疗药物的原料药、中间体服务单。除了在药物研发阶段,这些企业还会得到代加工订单,接下来,在新冠肺炎治疗药物走向获批上市阶段后,也将会实现巨大的商业附加利益,毕竟全球新冠肺炎患者数量较为庞大。
而安永大中华区生命科学与医疗健康行业联席主管合伙人吴晓颖此前在接受21世纪经济报道记者采访时也指出,在新冠全球大流行的背景下,市场寄希望于新冠疫苗+新冠病毒治疗药物的组合可以使得新冠 “流感化”。 如此也会使得短期内由于中国原料药在全球供应链中的地位以及良好的国内疫情管控,部分和跨国药企深度合作的原料药生产厂商已经收获第一波业务机会,而长远看,随着市场趋于常态,越来越多的小分子药物上市使得价格回归合理区间,假设新冠口服小分子市场在百亿美金规模,5%-6%原料药市场,带来新的市场空间约为每年5-6亿美金。
(作者:季媛媛 编辑:徐旭)
21世纪经济报道及其客户端所刊载内容的知识产权均属广东二十一世纪环球经济报社所有。未经书面授权,任何人不得以任何方式使用。详情或获取授权信息请点击此处。