21世纪经济报道记者季媛媛 见习记者韩利明 上海报道 2023年,对生物制药企业来说挑战与机遇并存。一方面,生物医药板块估值处于历史相对低位;另一方面,随着医保政策整体进入优化阶段,叠加老龄化趋势加剧、公众健康意识提升等因素,医药行业也在持续释放回暖信号。
近期,生物制药上市企业陆续交出2023年“成绩单”。截至4月29日收盘,据21世纪经济报道记者初步统计,化学制药和生物制品两大板块,共有201家A股上市公司发布2023年年报。其中,超七成企业实现盈利。
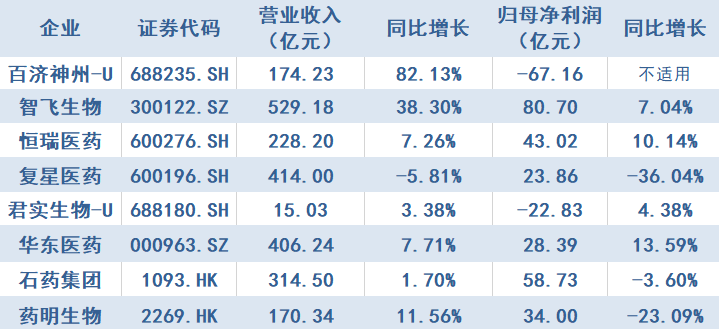
相同指标下,港股市场共有56家公司发布2023年年报。2023年盈利企业占整体比重超41%。其中,化学制药板块,石药集团实现归母净利润58.73亿元;生物制品板块,药明生物实现归母净利润约34亿元,分别在各自板块中排名首位。
(部分上市药企2023年业绩 数据来源:药企年报 数据整理:韩利明)
2024年或是未来三年医药新周期的起点。国信证券在研报中分析,随着国内医药公司研发投入逐步兑现,以A股医药上市公司为例,预计未来3年收入增长在10%~15%之间,若扣非利润率提升2个点,则未来3年医药行业的扣非利润有望增长75%,年化复合增长在20%以上。创新药企、具有国际化能力及潜力的公司等将成为关注重点。
迪哲医药董事长、总经理张小林对21世纪经济报道记者表示,创新药研发具有高投入、高风险、长周期的特点。近年来,从国家层面到地方层面,为生物医药的高质量发展出台了诸多扶持和鼓励政策。近期,北京、广州一系列鼓励政策的出台,有助于促进创新药企加快研发速度,减轻资金压力。
“高质量”成为生物制药行业发展的关键词之一。4月23日至24日,国家药品监督管理局党组书记、国家药品监督管理局局长李利在上海市有关医药企业考察调研时强调,“生物医药是全球新一轮科技革命和产业变革的重点方向,是新质生产力的重要组成,是推动经济高质量发展的重要领域。”
加大研发投入
2023年,创新能力不足的企业面临更大的生存挑战,源头创新产品的发展加速,也需要企业真金白银投入。2023年内,上述A股生物制药上市公司研发费用合计高达708.93亿元。其中,超过140家药企加大了研发投入。
在A股化学制药板块中,恒瑞医药实现归母净利润43.02亿元,研发费用49.54亿元,两项指标均排名首位。生物制品板块中,智飞生物实现净利润80.7亿元,百济神州投入研发费用128.13亿元,分别在各自指标中排名首位。
生物制药行业的高研发投入正在逐渐兑现成果。国家药品监督管理局药品审评中心数据显示,2023年,全年共有40个1类创新药获批上市其中9个品种为通过优先审评审批程序批准上市,13个品种为附条件批准上市,8个品种在临床研究阶段纳入了突破性治疗药物程序、4个新冠治疗药物通过特别审批程序批准上市。
其中,恒瑞医药在2023年内共有3款1类创新药(阿得贝利单抗、磷酸瑞格列汀、奥特康唑)、4款2类新药(盐酸右美托咪定鼻喷雾剂、醋酸阿比特龙纳米晶、盐酸伊立替康脂质体、恒格列净二甲双胍缓释片)获批上市。
百济神州2023年年报显示,同行业平均研发投入金额为15.71亿元,百济神州的研发投入是该数字的8倍之多。目前,百济神州共有3款自主研发并获批上市的药物,包括百悦泽®(泽布替尼)、百泽安®(替雷利珠单抗)和百汇泽®(帕米帕利)。其中,百悦泽®实现营业收入91.38亿元(约13亿美元),成为国内首个年销售额超过十亿美元的国产创新药。
差异化布局
从研发管线来看,2023年内,抗肿瘤药物仍是全球药物研发的重中之重。本土药企的创新研发能力也逐步获得认可,对外许可交易为多家上市药企贡献重要的现金流来源。其中,以ADC为代表的药物类型在2023年内大放异彩。
例如科伦博泰于2022年将其具有自主知识产权的靶向TROP2的创新ADC药物即“SKB264(MK2870)项目”有偿独家许可给默沙东进行中国以外区域范围内的研究、开发、生产制造和商业化,合作总金额超100亿美元。
此外,2023年12月,百利天恒就自主研发的一款双抗ADC(BL-B01D1)抗肿瘤药物,与百时美施贵宝(BMS)达成独家许可与合作协议,潜在总交易额最高可达84亿美元。该笔交易刷新了全球ADC类药物单品交易总价的记录。百利天恒年报披露,在2024年3月已收到由BMS支付的8亿美元首付款。
麦肯锡全球资深董事合伙人王锦在接受21世纪经济报道记者采访时表示,2023年,在中国创新产品对外授权交易中,一半左右是聚焦新一代的技术平台(如ADC)。另外一个数据也验证了中国在全球技术平台创新中的优势,源自中国的抗体偶联药物(ADC)在全球针对ADC这一技术平台的共33个对外授权交易中贡献了10个授权交易。
“中国在技术平台上突出优势来自于两方面,一是工程优势,也就是在现有技术的快速迭代,依托于强大的理工科人才和技术能力储备;二是中国速度和规模,采用有韧性、效率为先的工作模式,以‘中国速度’快速生成临床和PoC数据。我相信中国企业有潜力将竞争优势延伸至其他技术平台和药物机理,例如双/多特异性抗体、细胞基因治疗(CGT)等。”王锦说。
2023年内,随着GLP-1发展成为全球热捧的减肥“网红”药物,国内不少上市药企布局该赛道。华东医药子公司中美华东的“利拉鲁肽注射液”于2023年7月4日获批新适应症,用于肥胖或超重,成为国内首个获批上市的GLP-1类减肥适应症药物。在华东医药披露的2023年年报中,虽未显示具体销售额,但华东医药直言“该产品上市以来销售势头良好,将为公司后续GLP-1类产品商业化奠定坚实基础。”
走稳“出海”路径
为了寻求更多的获利和市场,“走出去”成为国内药企公认的发展策略。
据21世纪经济报道记者梳理,2023年下半年以来,我国共有3款创新药获得FDA批准上市,证明在临床上有差异化,切实针对海外未被满足的临床需求的产品具备进入美国市场的能力。包括君实生物的特瑞普利单抗(PD-1单抗,Loqtorzi)、和黄医药的呋喹替尼(VEGFR1/2/3抑制剂,Fruzaqla)、亿帆医药的艾贝格司亭α注射液(Ryzneuta)。
综合这三家企业2023年年报,报告期内,特瑞普利单抗实现销售收入约9.19亿元,同比增长约25%;呋喹替尼的市场销售额增长15%至1.075亿美元;亿帆医药称艾贝格司亭α注射液作为公司首个在中美欧获批的创新生物药,2024年将迈入商业化的关键年份。
“出海”之路“风高浪急”,选择适合自己的出海方式十分重要,其中造船出海、license-out(借船出海)、联合出海是常见的三种方式。
和黄医药资深副总裁崔昳昤在接受21世纪经济报道采访时直言,“起初和黄医药是‘造船出海’,前两年尝试在美国建立临床和销售团队,但后来判断,短期内更适合‘借船出海’。此外,美国食品药品监督管理局的审批标准和国内有差异,商业化团队的建立不是一蹴而就的,既需要掌握当地的准入政策,也需要了解美国的医院和医保体系。”
在此考虑下,和黄医药与武田达成独家许可协议,在全球范围内进一步推进呋喹替尼的开发、商业化和生产。和黄医药2023年年报披露,和黄医药肿瘤/免疫业务综合收入增长223%至5.286亿美元,接近财务指引上限,包括确认自武田收取的首付款中的2.8亿美元。
更多的创新药企在加速“出海”布局。张小林对21世纪经济报道记者表示,随着大部分创新药企盈利能力的提升,“行业寒冬”终会结束。对于创新药企来说,想在未来的竞争中取得领先,既要在研发端具备以临床价值为导向的高质量创新实力,开发具有差异化竞争优势的产品,又要在市场端具备高效的商业化能力。
但出海策略带来协同效应的同时,也有不少药企在走向国际化过程中遭遇实操难题。例如2023年2月15日,诺诚健华宣布,渤健已通知公司,为便利而终止(Terminate for Convenience)双方就奥布替尼的全球开发和商业化达成的合作和许可协议。诺诚健华2023年年报显示,5月已与渤健已完成相关权益过渡,报告期内,奥布替尼销售额为6.71亿元,较2022年同比增长18.52%。
创新药“出海”任重道远,但可以预见的是,走全球化道路仍是必经之路。
(作者:季媛媛,韩利明 编辑:包芳鸣)
南方财经全媒体集团及其客户端所刊载内容的知识产权均属其旗下媒体。未经书面授权,任何人不得以任何方式使用。详情或获取授权信息请点击此处。